Nos estertores de 2019, o mundo foi apresentado àquele que seria, em bem pouco tempo, seu maior inimigo. Cinco meses depois, a Covid-19 já é a maior pandemia desde a gripe espanhola, com mais de 186 mil mortes confirmadas até o dia 23 de abril. Desde o break out da doença, cientistas e pesquisadores do mundo todo não medem esforços para encontrar uma cura ou ao menos uma forma de reduzir seus impactos. A solução definitiva ainda não chegou, mas o protocolo seguido globalmente tem seguido o mesmo roteiro: testar, tratar e buscar a cobiçada vacina.
A importância de testar a população, para o especialista em doenças infecciosas Celso Granato, diretor clínico do Grupo Fleury, é a possibilidade de entender a dinâmica da pandemia e assim escolher os melhores caminhos na contenção do contágio. “É importante testar a população tanto para sabermos o número de infectados como para conhecermos individualmente quem já está imunizado e pode voltar à rotina”, diz Granato. Estudos recentes demonstram que pessoas curadas da Covid-19 até podem voltar a apresentar traços do vírus em exames moleculares, mas o vírus encontrado nessas pessoas é “defeituoso” e não oferece mais riscos de contágio.
Há hoje dois tipos de teste: o molecular, conhecido como RT-PCR, que encontra dentro do organismo testado traços do vírus em si; e os testes sorológicos, que detectam nos organismos testados os anticorpos específicos do vírus. Ambos são considerados eficientes e servem a diferentes finalidades: o teste molecular é mais recomendado para quem já está apresentando sintomas, e a sorologia é recomendada para quem ainda não apresenta sintomas, mas quer saber se já possui ou não os anticorpos (se está teoricamente imunizada).
A dificuldade que os países enfrentam é o retardo na produção em massa dos testes e a escassez dos insumos necessários à sua produção. “Nós sabemos que é preciso testar, mas vamos testar com quê? Não temos uma indústria capaz de suprir essa demanda da noite para o dia”, diz Granato.
Medidas paliativas
Outra grande questão que surgiu em relação à Covid-19 gira em torno dos medicamentos apontados como alternativa para amenizar os efeitos do vírus nas pessoas contaminadas. A cloroquina, o agora famoso remédio contra malária que tem sido usado no tratamento da Covid-19, levantou polêmicas em vários países. Alguns estudos apontam que a cloroquina e a hidroxicloroquina, sua versão menos tóxica, combinadas com o zinco e a azitromicina, são uma opção barata e eficiente para tratar a doença; outros trabalhos dizem o contrário.
No Brasil, a oncologista Nise Yamaguchi, que chegou a ser cotada para o Ministério da Saúde, defende o uso desses medicamentos combinados nos primeiros sintomas da doença. “A grande questão é sobre o grau de eficiência dos medicamentos. A cloroquina atua como antiviral e a azitromicina age como antibiótico e como antiviral. Precisamos aguardar mais pesquisas para termos certeza, mas, durante a epidemia, podemos nos perguntar qual é o risco de se morrer de uma grande infecção quando você tem a chance de tratar a viremia, quando ele ainda está se proliferando e se multiplicando”, explica ela. A vantagem de tratar os pacientes nesse estágio é diminuir o número de contaminados que evoluem o quadro a ponto de necessitarem de internação em UTIs e, assim, diminuir a pressão nos sistemas de saúde.
A cada dia surgem novas pesquisas acerca de remédios supostamente eficazes no tratamento da doença. Entre elas, um estudo da Monash University em parceria com o Instituto de Imunologia e Infecção Doherty, ambos da Austrália, que indica que uma droga usada contra verminoses é eficiente contra o novo coronavírus (esse estudo ainda não pode ser usado com segurança em humanos).
No Brasil, o ministro da Ciência e Tecnologia, Marcos Pontes, afirmou, no dia 20 de abril, que “um remédio” obteve 94% de sucesso em testes e deve ser disponibilizado à população em maio, depois de passar por uma fase final de testes durante a qual 500 pacientes candidatos serão tratados. O remédio, que até então era tratado como “secreto”, seria o antiparasitário nitazoxanida, fabricado no Brasil por grandes laboratórios, como Eurofarma, Medley e Aché. Assim como a cloroquina, foi alvo de controvérsia – e, por via das dúvidas, a Anvisa resolveu frear uma possível corrida às farmácias, passando a exigir receita médica em duas vias.
VEJA TAMBÉM: Como estão as pesquisas de 26 farmacêuticas em medicamentos e vacinas para a Covid-19
O antiviral Remdesivir, desenvolvido pela empresa norte-americana Gilead Sciences para o tratamento de ebola e Mers, também está em fase de testes para o tratamento da doença em diferentes lugares. Na última semana de abril, no entanto, o resumo de um estudo chinês divulgado “acidentalmente” no site da OMS e replicado pelo “Financial Times” dizia que não foi observada melhora nas 158 pessoas tratadas com o medicamento.
Em busca da cura
Além das medidas de contenção imediata, com foco na descoberta do melhor tratamento dos sintomas, a vacina é o santo graal da indústria farmacêutica. Segundo o chefe do Laboratório de Imunologia do Incor (Instituto do Coração do Hospital das Clínicas da FMUSP) em São Paulo, Jorge Kalil, o processo de criação de uma vacina, da bancada até a ampola pronta para consumo, pode levar até 15 anos. O imunologista está à frente de uma pesquisa promissora nesse sentido – e avalia ser “impossível” que o mundo conheça uma vacina ainda no ano de 2020, por maiores que sejam os investimentos.
Kalil conta que sua pesquisa recebeu um aporte de R$ 4,5 milhões do Ministério da Ciência e Tecnologia, mas ainda precisa de recursos. “Quero chegar pelo menos ao fim da primeira etapa da fase clínica com sucesso. Se eu chegar lá e provar que minha vacina teve êxito, o dinheiro virá”, diz ele.
A pesquisa que Kalil lidera aborda uma técnica específica. “É tudo uma questão de estratégia científica, cada pesquisador procura um caminho. Nós escolhemos o nosso: estamos sintetizando um arcabouço do vírus, e nessa casca do ovo, que é oca, enxertamos aquilo que acreditamos ser o melhor alvo para estimular a produção de anticorpos pelo organismo”, explica o médico. “Não é uma coisa clara de fazer. Estamos sintetizando os fragmentos com os quais queremos gerar anticorpos. Devemos iniciar em breve os testes em animais. Se tudo der certo, vamos iniciar a fase clínica no início do ano que vem”, afirma.
Além do Incor, a Fiocruz também está na corrida pela vacina made in Brazil. Apoiada por outras instituições (como UFMG e Instituto Butantan) e liderada pelos pesquisadores Alexandre Machado e Ricardo Gazzinelli, sua linha de pesquisa consiste em manipular o vírus influenza, tornando-o inócuo, e inserir nele sequências genéticas do novo coronavírus, gerando uma vacina bivalente que produzirá anticorpos para ambos os patógenos: influenza e Covid-19. “Acreditamos que até o fim do ano o mundo já terá passado pela pandemia. Então, as pessoas perguntam: por que criar uma vacina se ela não estará pronta a tempo? A resposta é que não sabemos o que vai acontecer no futuro, precisamos evoluir as pesquisas para estarmos preparados. Adaptar uma vacina pronta é infinitamente mais rápido do que criar uma do zero. A H1N1 foi contida, em grande parte, porque já havia outras vacinas contra o influenza que puderam ser adaptadas rapidamente”, explica Machado. Para o desenvolvimento dessa pesquisa, o grupo recebeu um aporte de R$ 6 milhões do Ministério da Ciência e da Fapemig (Fundação de Amparo à Pesquisa do Estado de Minas Gerais). Deve ficar pronta para testes em animais no segundo semestre deste ano. Depois é que vem o verdadeiro gargalo: a produção e distribuição em larga escala.
“Há no mundo grupos que investiram cerca de US$ 1 bilhão para a criação das vacinas. Mas eles estão correndo atrás tanto como nós. Só não sabemos quem está indo na direção certa”, diz Kalil. “É importante entender que a corrida é contra o vírus e não entre os pesquisadores”, diz o pesquisador Alexandre Machado. Mas ele admite que há grandes benefícios para quem chegar primeiro. “É basicamente uma questão geopolítica: esse país poderá não só vacinar sua população primeiro como também vai recuperar a economia antes dos outros – além de poder controlar para quem vai distribuir sua vacina, quando e como. Ciência é poder.”
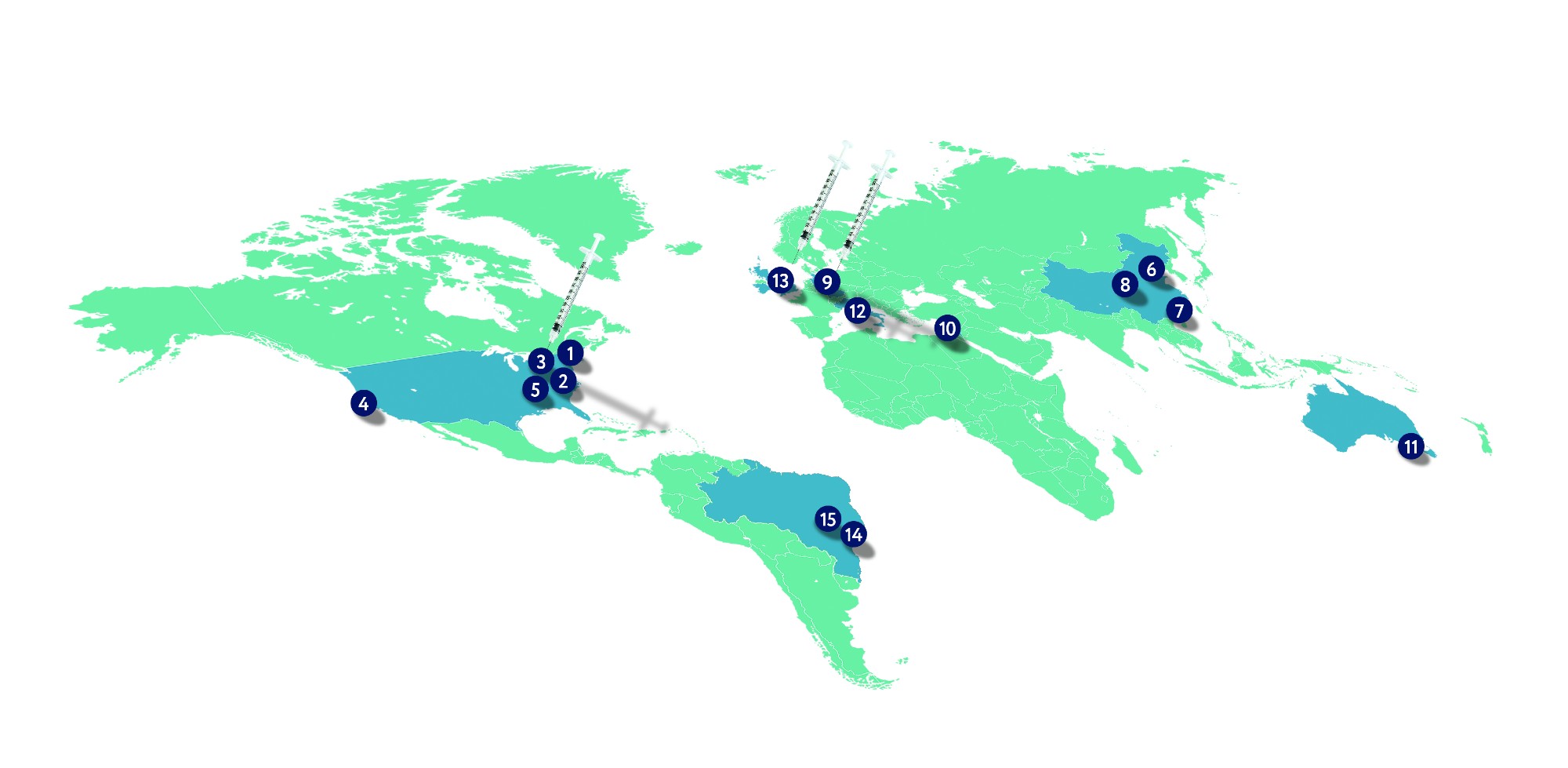
A CORRIDA PELA VACINA
ESTADOS UNIDOS
1. Moderna
A vacina do laboratório Moderna está em fase clínica. O primeiro candidato recebeu uma dose experimental no dia 16 de março. O laboratório receberá um aporte de US$ 483 milhões para a segunda fase do estudo, que deve ser iniciada ainda neste trimestre; a terceira fase está prevista para o terceiro trimestre de 2020.
2. Inovio
A empresa de biotecnologia Inovio Pharmaceuticals está sendo financiada pela Fundação Bill & Melinda Gates. Chamada de INO-4800, foi a segunda vacina americana a entrar em fase clínica, com os primeiros testes (em 40 candidatos) na segunda semana de abril.
3. Johnson & Johnson
Em parceria com a Autoridade Biomédica de Pesquisa e Desenvolvimento Avançado (Barda), a J&J investiu cerca de US$ 1 bilhão na busca de sua fórmula de imunização. Espera começar os testes clínicos até setembro de 2020.
4. Vaxart
A empresa sediada em South San Francisco anunciou no dia 21 de abril o sucesso de sua vacina em fases pré-clínicas. Ainda não há previsão para o início da fase clínica.
5. Novavax
Depois de testar com sucesso em animais, a empresa de biotecnologia anunciou em abril que iniciará a fase clínica da vacina em maio em um grupo de 130 candidatos. Espera os primeiros resultados em julho.
CHINA
6. CanSino Biologics
A empresa, com sede em Tianjin, está desenvolvendo em parceria com o Instituto de Biotecnologia de Pequim uma vacina candidata que está sendo testada desde março e que já entrou na segunda etapa da fase clínica, para a qual recrutou 500 candidatos.
7. Sinovac Biotech
O grupo farmacêutico Sinovac recebeu autorização para iniciar testes em humanos em 14 de abril.
8. Instituto de Produtos Biológicos de Wuhan
O instituto, em parceria com o grupo Sinopharm, recebeu autorização para iniciar os testes em humanos em 14 de abril.
ALEMANHA
9. BioNTech/Pfizer
A BioNTech, em parceria com a Pfizer, mantém um programa chamado BNT162 que tem quatro vacinas em estudo. Os testes iniciais, que tiveram aprovação do órgão regulador alemão no dia 22 de abril, serão feitos com 200 candi-datos saudáveis de 18 a 55 anos.
ISRAEL
10. Instituto de Pesquisa da Galileia
O doutor Chen Katz lidera uma das pesquisas israelenses e espera que a vacina esteja pronta para iniciar a fase clínica em 1º de junho.
AUSTRÁLIA
11. Instituto de Pesquisa Murdoch’s Children
O Murdoch’s Children vai conduzir um teste clínico para observar a eficácia da vacina BCG contra a Covid-19. A primeira fase do estudo aplicará 4 mil doses nos candidatos.
ITÁLIA
12. Takis Biotech
A startup anunciou no dia 10 de abril que suas cinco vacinas candidatas apresentaram bons resultados nos testes em animais. A Takis está captando investimentos para levar os testes às etapas da fase clínica até o fim do ano.
REINO UNIDO
13. Oxford e London Imperial College
O secretário de Saúde do Reino Unido, Matt Hannock, aprovou o início da fase clínica do grupo de Oxford. A primeira fase envolverá 500 candidatos. Para isso, o governo britânico disponibilizou cerca de R$ 280 milhões.
BRASIL
14. Incor
Está sintetizando fragmentos com os quais vai gerar anticorpos e iniciar os testes em animais.
15. Fiocruz
Sua tática é manipular o vírus influenza e inserir nele sequências genéticas do novo coronavírus.123456791011121381415
Reportagem publicada na edição 77, lançada em maio de 2020
Facebook
Twitter
Instagram
YouTube
LinkedIn
Participe do canal Forbes Saúde Mental, no Telegram, e tire suas dúvidas.
Baixe o app da Forbes Brasil na Play Store e na App Store.
Tenha também a Forbes no Google Notícias.