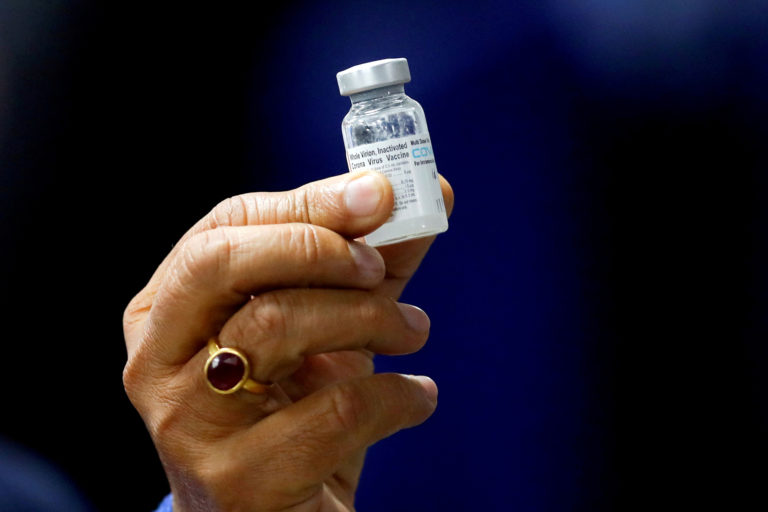
A vacina indiana Covaxin (foto) terá que cumprir com diversos requisitos caso sua importação seja aprovada pela diretorias da Anvisa
A área técnica da Agência Nacional de Vigilância Sanitária (Anvisa) disse hoje (4) que ainda há “incertezas técnicas” com relação às vacinas contra Covid-19 Sputnik V, da Rússia, e Covaxin, da Índia, e recomendou uma série de condicionantes caso a importação dos imunizantes seja aprovada pela diretoria do órgão.
Em seu parecer, o gerente-geral de Medicamentos e Produtos Biológicos do órgão, Gustavo Mendes, ressaltou que a área técnica da Anvisa não está atestando a qualidade, segurança e eficácia das duas vacinas, mas apresentando seu parecer conforme determina uma lei sobre a importação emergencial de vacinas por ocasião da pandemia.
VEJA TAMBÉM: Brasil pode receber 3 milhões de doses da vacina da Janssen em junho
“Existem pendências técnicas que precisam ser resolvidas“, afirmou. “Contudo, a lei existe, a lei foi pensada no contexto da pandemia. Há recomendação de que o uso seja controlado, que sejam observados com muito cuidado os resultados que serão gerados com esse uso.”
Para ambas as vacinas, a área técnica da Anvisa destacou a necessidade de aprovação pelo Instituto Nacional de Controle de Qualidade em Saúde (INCQS) para atestar a segurança e eficácia dos imunizantes.
Os dois imunizantes só devem ser usados em pessoas saudáveis, disse a área técnica, e as doses enviadas ao Brasil precisam ser provenientes de instalações que foram vistoriadas pela agência reguladora, caso as importações sejam aprovadas.
As recomendações da área técnica do órgão regulador serão levadas em conta para a decisão que a diretoria colegiada fará sobre o pedido de importação ainda nesta sexta.
A Anvisa havia rejeitado em abril pedido de importação da vacina russa feita por governadores após a área técnica da agência listar uma série de “deficiências” no pedido e afirmar que não poderia ser avalizada a importação em razão da falta de informações mínimas para se garantir uma análise da segurança, qualidade e eficácia do imunizante.
Agora, a área técnica da Anvisa fez uma nova análise com base em relatório do Ministério da Saúde da Rússia, que concedeu o registro condicional para a vacina.
Ao todo, os governadores que pediram a aprovação da importação à Anvisa têm pré-contratos para aquisição de 65 milhões de doses da Sputnik, enquanto o governo federal planeja comprar outras 10 milhões de doses.
No caso da Covaxin, a Anvisa havia rejeitado em março pedido de importação da vacina indiana feito pelo Ministério da Saúde, quando citou como um dos principais aspectos para a decisão a falta de um certificado de Boas Práticas de Fabricação pela Bharat.
Segundo a Anvisa, o Ministério da Saúde e a empresa Precisa Medicamentos, que representa a Bharat no Brasil, seguiram em tratativas com a Anvisa a fim de adequar os aspectos que motivaram a recusa e, nesse sentido, já foi publicada pela agência reguladora anuência para realização do estudo clínico com a vacina Covaxin no Brasil.
O governo federal tem um acordo para aquisição de 20 milhões de doses da Covaxin. (Com Reuters)
Siga FORBES Brasil nas redes sociais:
Facebook
Twitter
Instagram
YouTube
LinkedIn
Siga Forbes Money no Telegram e tenha acesso a notícias do mercado financeiro em primeira mão
Baixe o app da Forbes Brasil na Play Store e na App Store.
Tenha também a Forbes no Google Notícias.
















