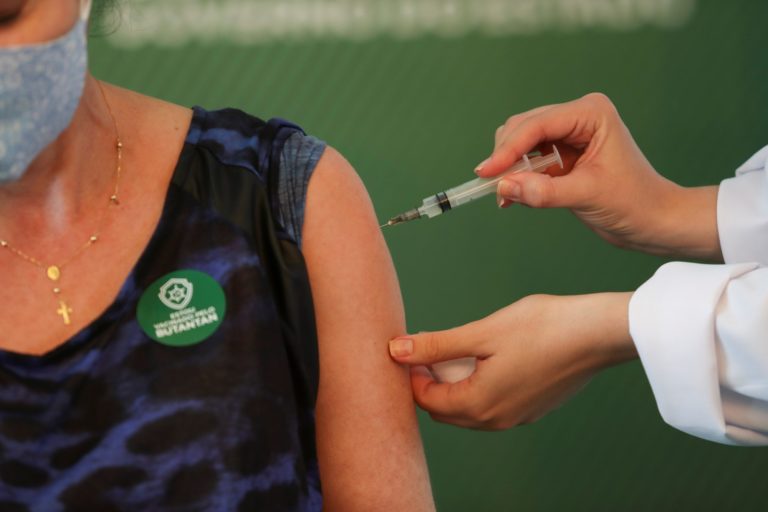
Dimas Covas disse que o Butantan aguarda autorização do governo chinês para a importação de insumos
O Instituto Butantan pedirá amanhã à Agência Nacional de Vigilância Sanitária (Anvisa) nova autorização para uso emergencial de mais 4 milhões de doses da CoronaVac, vacina contra Covid-19 do laboratório chinês Sinovac, disse hoje (17) o presidente do instituto, Dimas Covas.
Em entrevista coletiva no Hospital das Clínicas, onde profissionais de saúde começaram a ser vacinadas contra a doença no Brasil, Covas também disse que o Butantan aguarda esta semana autorização do governo chinês para a importação de insumos que serão usados no envase de mais 11 milhões de doses do imunizante, que teve sua primeira autorização para uso emergencial dada pela Anvisa neste domingo.
VEJA TAMBÉM: Brasil deve receber esta semana doses da vacina da AstraZeneca vindas da Índia
“Amanhã, segunda-feira, nós entramos na Anvisa com o pedido de autorização para uso emergencial para as vacinas produzidas aqui no Butantan, das quais já temos 4 milhões de doses prontas e necessitamos agora a urgência de nova autorização. Como a documentação é praticamente a mesma, não existe muita diferença, isso seja aprovado muito rapidamente”, disse Covas.
“Estamos com um pedido aprovado de importação lá na China e neste momento aguardamos uma autorização do governo chinês. Isso já deveria ter acontecido 15 dias atrás, não aconteceu, estamos em intenso contato com os chineses para que liberem essas doses, que serão suficientes para a produção de mais de 11 milhões de doses… Esperamos que isso se resolva nesta semana ainda.”
Durante a votação da diretoria colegiada da Anvisa, que deu autorização para uso emergencial à CoronaVac e à vacina da AstraZeneca em parceria com a Universidade de Oxford, a agência também disse que o Butantan deveria enviar um termo se comprometendo a enviar dados de imunogenicidade da vacina até fevereiro.
Indagado sobre o assunto na coletiva, Covas disse que já enviou o termo à Anvisa e, embora tenha questionado a exigência, disse que o Butantan cumprirá com ela.
“Quando eu pedi licença ao governador para me ausentar por alguns minutos (da coletiva) foi justamente para assinar esse documento que a Anvisa enviou. Está assinado e devolvido”, afirmou.
“Os dados de imunogenicidade foram oferecidos para a Anvisa. Na realidade o que consta é que eles querem que repita os testes de imunogenicidade com outro kit. Na realidade é isso… Embora isso não se justifique do ponto de vista técnico –tenho argumentado isso já há algum tempo– faremos isso sem problema algum. Isso faz parte, atenderemos a essa exigência muito rapidamente.” (Com Reuters)
Siga FORBES Brasil nas redes sociais:
Facebook
Twitter
Instagram
YouTube
LinkedIn
Siga Forbes Money no Telegram e tenha acesso a notícias do mercado financeiro em primeira mão
Baixe o app da Forbes Brasil na Play Store e na App Store.
Tenha também a Forbes no Google Notícias.
















