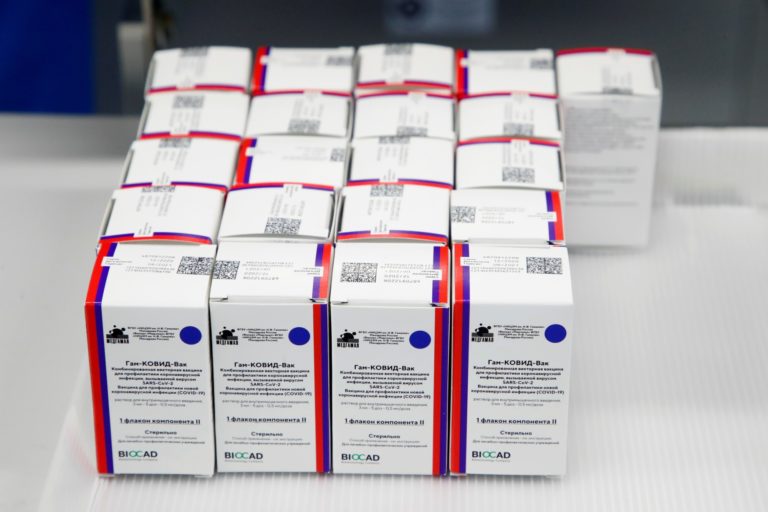
A Anvisa (Agência Nacional de Vigilância Sanitária) recebeu ontem (31) complementação ao pedido para uso emergencial da vacina Sputnik V, encaminhado pela União Química Farmacêutica, informou nota da agência hoje (1), mas ainda faltam documentos e o prazo de análise segue suspenso.
O pedido de uso emergencial no Brasil da Sputnik V, vacina contra Covid-19 desenvolvida pelo Instituto Gamaleya de Moscou, foi recebido pela Anvisa na última sexta-feira (26). Mas diante da ausência de documentos considerados importantes, a agência suspendeu, no domingo (28), o prazo de análise do pedido de autorização para uso emergencial.
LEIA MAIS: Vacina da Pfizer oferece alta proteção contra variante sul-africana do coronavírus
Segundo a nota da agência reguladora de hoje, os documentos recebidos fazem parte de item que trata dos requisitos mínimos para autorização de uso emergencial, que “trata da lista de todos os locais onde a vacina está ou será fabricada, e as documentações relacionadas às Boas Práticas de Fabricação (BPF) dos locais de fabricação”.
A Anvisa acrescentou, no entanto, que ainda falta a entrega de documentos relacionados a outros itens que também tratam de Boas Práticas de Fabricação, razão pela qual “o prazo de sete dias úteis permanece suspenso até a apresentação da documentação faltante”.
De qualquer forma, a agência esclareceu que o material já enviado é avaliado pela equipe técnica. (Com Reuters)
Siga FORBES Brasil nas redes sociais:
Facebook
Twitter
Instagram
YouTube
LinkedIn
Siga Forbes Money no Telegram e tenha acesso a notícias do mercado financeiro em primeira mão
Baixe o app da Forbes Brasil na Play Store e na App Store.
Tenha também a Forbes no Google Notícias.