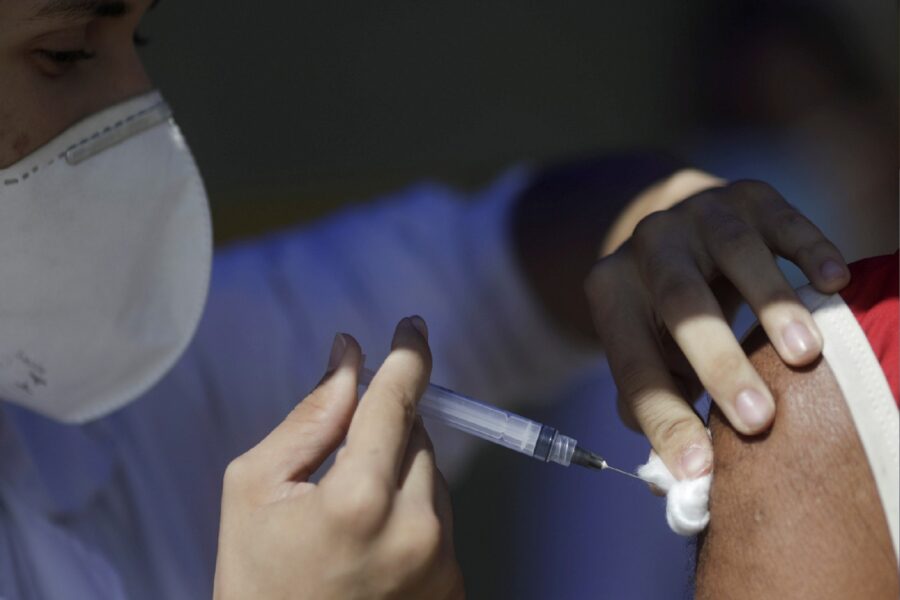
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou hoje (19) a realização de um estudo para medir a segurança e a eficácia de uma terceira dose da vacina contra Covid-19 da AstraZeneca, informou o órgão regulador em nota.
De acordo com a Anvisa, o estudo, patrocinado pela AstraZeneca, será feito com os participantes da pesquisa inicial que receberam as duas doses da vacina com um intervalo de quatro semanas entre elas. A terceira dose será aplicada entre 11 e 13 meses após a segunda dose.
LEIA TAMBÉM: Primeiro caso de Covid-19 na Vila Olímpica aumenta a pressão sobre o COI
O estudo será feito somente no Brasil com 10 mil voluntários na Bahia, Rio de Janeiro, Rio Grande do Sul, Rio Grande do Norte e São Paulo, segundo nota da Anvisa.
A agência também informou que autorizou estudo clínico para avaliar a segurança e eficácia do medicamento Proxalutamida na redução da infecção viral causada pelo novo coronavírus e no processo inflamatório provocado pela Covid-19.
Este estudo será feito em participantes ambulatoriais do sexo masculino com Covid-19 leve a moderada e é patrocinado pela empresa chinesa Suzhou Kintor Pharmaceuticals.
A pesquisa será realizada na Alemanha, Argentina, África do Sul, Ucrânia, México, Estados Unidos e no Brasil, onde participarão 12 voluntários no Estado de Roraima e outros 38 em São Paulo. (Com Reuters)
Facebook
Twitter
Instagram
YouTube
LinkedIn
Siga Forbes Money no Telegram e tenha acesso a notícias do mercado financeiro em primeira mão
Baixe o app da Forbes Brasil na Play Store e na App Store.
Tenha também a Forbes no Google Notícias.










