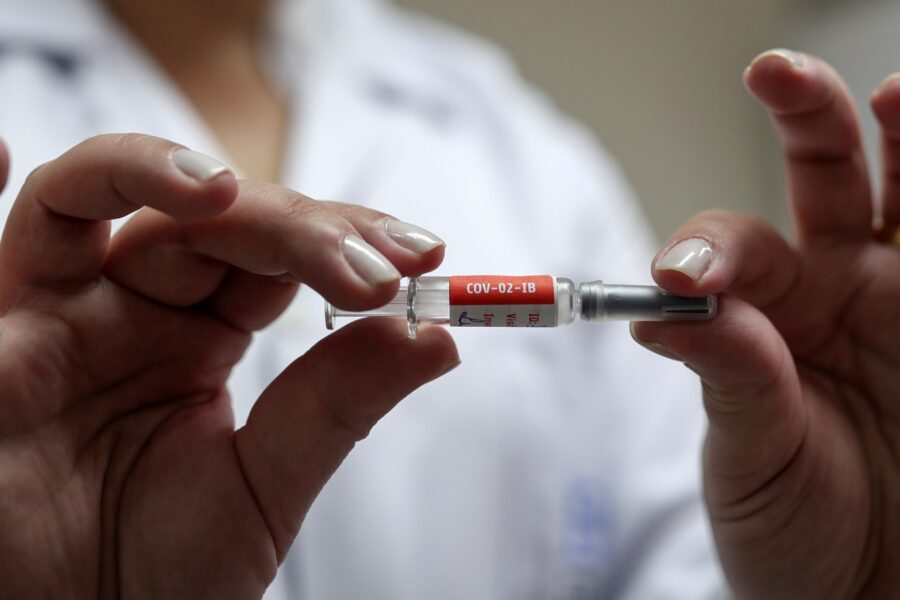
A Agência Nacional de Vigilância Sanitária (Anvisa) anunciou hoje (8) que recebeu o pedido para uso emergencial no país da CoronaVac, potencial vacina contra Covid-19 do laboratório chinês Sinovac, feito pelo Instituto Butantan, responsável pelos testes com o imunizante no Brasil.
“A meta da Anvisa é fazer a análise do uso emergencial em até 10 dias, descontando eventual tempo que o processo possa ficar pendente de informações, a serem apresentadas pelo laboratório”, afirmou a Anvisa em nota.
LEIA MAIS: Ministério da Saúde assina acordo com Butantan por 100 milhões de doses da CoronaVac
Também em nota, o Butantan confirmou que deu entrada no pedido, afirmando que foi feito às 9h34 de hoje e reiterando também o prazo dado pela Anvisa de 10 dias para uma análise.
Na véspera, o Butantan anunciou que a CoronaVac teve eficácia de 78% na prevenção da Covid-19 em estudo clínico de Fase 3 feito no Brasil e que mostrou ser 100% eficaz contra casos graves e moderados da doença.
A solicitação do Butantan à Anvisa faz da CoronaVac a primeira vacina contra Covid-19 a ter o pedido para uso emergencial feito no Brasil. (Com Reuters)
Siga FORBES Brasil nas redes sociais:
Facebook
Twitter
Instagram
YouTube
LinkedIn
Siga Forbes Money no Telegram e tenha acesso a notícias do mercado financeiro em primeira mão
Baixe o app da Forbes Brasil na Play Store e na App Store.
Tenha também a Forbes no Google Notícias.










