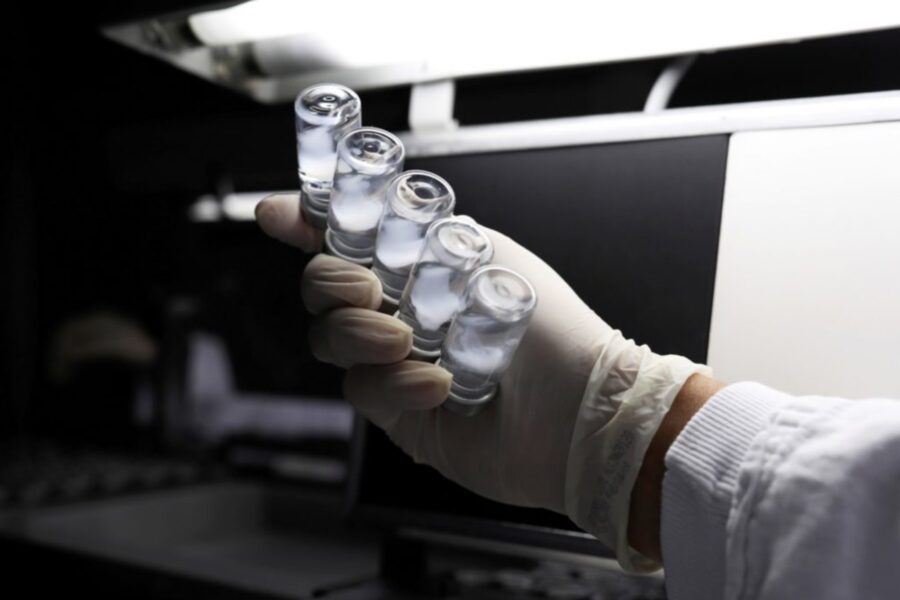
O Instituto Butantan anuncia hoje (26) o pedido de autorização à Anvisa (Agência Nacional de Vigilância Sanitária) para iniciar os testes em humanos de uma potencial vacina contra a Covid-19 desenvolvida pelo instituto ligado ao governo do Estado de São Paulo, disseram à Reuters duas fontes a par do assunto.
Os estudos de Fases 1 e 2 contarão com 1.800 voluntários. A potencial vacina, batizada de Butanvac, é uma iniciativa de um consórcio internacional liderado pelo Butantan, e o imunizante será 100% desenvolvido no Brasil, se acordo com uma das fontes.
LEIA MAIS: Pfizer e BioNTech iniciam teste de vacina contra Covid-19 em crianças menores de 12 anos
O instituto paulista deterá 85% da capacidade total de produção entre os membros do consórcio e, além do Brasil, a ideia é fornecer a Butanvac a países de renda baixa e média.
O anúncio oficial está sendo feito em coletiva de imprensa, marcada para 8h desta manhã, na sede do Butantan, na zona oeste de São Paulo, com a presença do governador do Estado, João Doria (PSDB), e do presidente do instituto, Dimas Covas.
A vacina usará a tecnologia de vírus inativado, que o Butantan domina, e a expectativa é que ela possa começar a ser produzida em escala maior (para além das doses usadas nos testes) a partir de maio, quando o instituto concluir a produção de doses da vacina da gripe para a campanha de imunização contra a doença, disse uma das fontes.
O desenvolvimento da nova vacina, segundo essa fonte, não altera o acordo que o Butantan tem com o laboratório chinês Sinovac para envase e futura produção no Brasil da CoronaVac. Nem mesmo os trabalhos de construção de uma nova fábrica para produção integral da vacina chinesa a partir de janeiro será afetado, ao menos por ora.
O objetivo, afirmou, é aumentar a oferta de vacinas e garantir independência ao Brasil no fornecimento de imunizantes, sem depender de compras no exterior.
Doria publicou um vídeo e um texto em sua conta no Twitter na noite de ontem (25) em que informa sobre a coletiva da manhã de hoje. “Mais uma vez, a ciência nos enche de esperança na luta contra a Covid-19”, afirmou sem entrar em detalhes do anúncio que será feito.
As primeiras duas fases de testes em humanos de uma vacina são realizadas com um número reduzido de voluntários e têm o objetivo de verificar se o imunizante é seguro e se induz o organismo a produzir a resposta imune esperada. Já na Fase 3, realizada em um número maior de voluntários, é testada a eficácia da vacina.
O Butantan realizou os testes da Fase 3 da CoronaVac no Brasil. O instituto já entregou 27,8 milhões de doses da vacina ao Programa Nacional de Imunização (PNI) do Ministério da Saúde. O contrato do Butantan com o ministério prevê a entrega de um total de 100 milhões de doses da CoronaVac até o final de setembro, prazo que o Butantan promete antecipar para agosto. (com Reuters)
Facebook
Twitter
Instagram
YouTube
LinkedIn
Siga Forbes Money no Telegram e tenha acesso a notícias do mercado financeiro em primeira mão
Baixe o app da Forbes Brasil na Play Store e na App Store.
Tenha também a Forbes no Google Notícias.










